

对映选择性烷基‒烷基交叉偶联是构建手性三维分子结构的一种有效策略,在有机化学和药物化学等领域至关重要。自由基‒自由基交叉偶联为此提供了一种新思路,并具有一定的优势。一方面,这种方法可使用来源广泛的自由基前体(如羧酸、卤化物、醇等),几乎允许以任何组合进行偶联;另一方面,自由基型偶联的反应条件较为温和且官能团耐受性良好。然而,由于自由基的瞬态性质,实现两个不同自由基之间偶联的交叉选择性和对映选择性控制仍然是一个巨大挑战。
近日,同济大学杨泽鹏课题组基于丰产金属催化不对称偶联反应的研究兴趣(J. Am. Chem. Soc. 2024, 146, 9404−9412; Nat. Commun. 2024, 15, 2733; Angew. Chem. Int. Ed. 2025, 64, e202506883; Sci. China. Chem. 2025, 68, doi:10.1007/s11426-025-2666-y),开发了一种光/镍协同催化的自由基‒自由基交叉偶联反应,成功实现了一系列含手性叔碳中心化合物的精准合成。相关研究成果“Enantioselective Radical‒Radical Cross-Couplings of β-Hydroxy Amides and N-Hydroxyphthalimide Esters via Ni/Photoredox Catalysis”在线发表于国际知名学术期刊《Journal of the American Chemical Society》。
在最优条件下,反应具有良好的底物普适性和官能团耐受性。作者通过一锅法反应、克级反应、偶联产物的转化和天然产物的合成展示了该方法的实用性。作者还对反应机理进行了较为深入的探究,提出了可能的催化循环。在碱的作用下,烷基醇和NHC(N-杂环卡宾盐)反应生成NHC醇的加合物;激发态的光催化剂[IrIII]*将NHC醇的加合物单电子氧化,生成阳离子自由基物种,接着经历去质子化和β裂解过程生成二级烷基自由基;被还原猝灭的光催化剂[IrII]具有较强的还原性,可以将NHP酯还原为一级烷基自由基;在镍催化循环中,一价镍溴中间体首先与一级烷基自由基结合生成二价烷基镍溴中间体;随后与二级烷基自由基反应(内球机制或外球机制)生成偶联产物,同时再生一价镍溴中间体,完成催化循环。
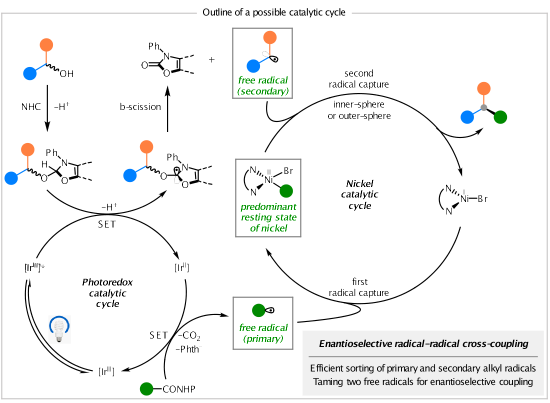
综上所述,杨泽鹏课题组实现了一种光/镍协同催化非活化β-羟基酰胺和烷基NHP酯的对映选择性自由基‒自由基交叉偶联反应。该反应的特点在于通过光氧化还原过程独立产生两个不同的烷基自由基物种,然后被手性二胺配体配位的镍催化剂选择性拦截,以实现良好的交叉和对映选择性。我院博士研究生张利利为论文第一作者,杨泽鹏教授为论文通讯作者。该研究工作得到了国家自然科学基金、科技部重点研发(青年)、上海市教委学科跃升计划、同济大学青年百人计划的资助。
课题组热忱欢迎对有机合成等领域感兴趣的有志青年加盟,开展创新实验、本科毕设、硕士博士攻读及博士后研究。
论文链接:https://doi.org/10.1021/jacs.5c10963
杨泽鹏课题组:https://zpyangorgchem.tongji.edu.cn/main.htm


